- Изучение новых CRISPR-Cas систем и их применение в биотехнологии
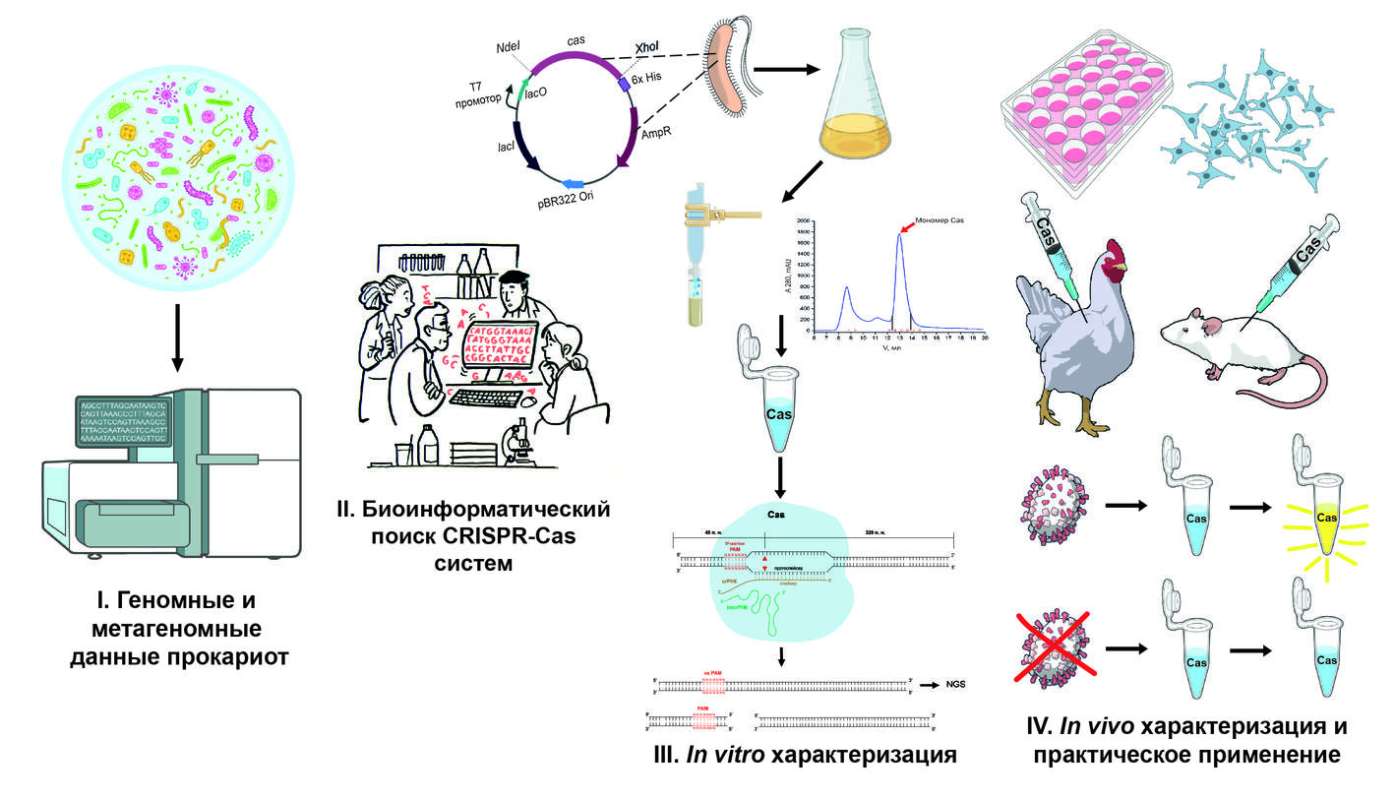
CRISPR-Cas – это система, обнаруженная у бактерий и архей, которая служит их естественным иммунитетом против вирусных инфекций. CRISPR-локус содержит повторяющиеся участки ДНК и спейсеры — фрагменты вирусной ДНК, с которыми клетки сталкивались ранее. При атаке вируса информация из CRISPR-локуса превращается в направляющие РНК, которые соединяются с белками Cas. Эти белки разрезают вирусную ДНК, обезвреживая вирус.
Главное научное открытие заключается в том, что этот природный механизм можно применять для редактирования геномов других организмов. Манипулируя направляющими РНК, ученые могут заставить Cas-белки целиться в строго определенные участки генома. Такое использование CRISPR-Cas систем стало мощным инструментом в молекулярной биологии.
Наша группа занимается поиском и исследованием новых CRISPR-Cas систем, открывая их в самых различных источниках. Мы работаем с тщательно изученными геномами и метагеномами из обширных баз данных, а также с уникальными образцами, которые нам предоставляют наши коллабораторы. Сначала с помощью компьютерного анализа (in silico) мы выделяем потенциальные CRISPR-Cas кандидаты. Как только подходящая система обнаружена, мы переходим к лабораторным испытаниям in vitro – проверяем, способен ли выбранный кандидат направленно разрезать предложенные нами фрагменты ДНК. Если система показывает активность, мы продолжаем работу двумя путями, в зависимости от целей. В первом случае мы тестируем систему in vivo, проверяя ее активность в культурах клеток человека. Это позволяет определить ее эффективность и потенциальное применение для редактирования генома. Во втором случае мы адаптируем CRISPR-Cas систему для использования в диагностике – она становится основой метода, который помогает быстро и точно определять наличие конкретных патогенов (бактерий и вирусов) в исследуемых образцах.
Наша цель – не просто изучение новых CRISPR-Cas систем, а их перевод в активное использование в исследовательских и практических приложениях.
Основные публикации:
1. Васильева А.А., Алюкас С.А., Селькова П.А., Арсениев А.Н., Чернова В.Е., Мушарова О.С., Климук Е.И., Ходорковский М.А., Северинов К.В. Нуклеазы CRISPR-Cas II типа: алгоритм поиска и in vitro характеристика // Молекулярная биология. – 2023. – Т. 57. – №3. – C. 546–560. doi: 10.31857/S0026898423030163
2. Vasileva A, Selkova P, Arseniev A, Abramova M, Shcheglova N, Musharova O, Mizgirev I, Artamonova T, Khodorkovskii M, Severinov K, Fedorova I. Characterization of CoCas9 nuclease from Capnocytophaga ochracea. RNA Biol. 2023 Jan;20(1):750-759. doi: 10.1080/15476286.2023.2256578
3. Fedorova I, Vasileva A, Selkova P, Abramova M, Arseniev A, Pobegalov G, Kazalov M, Musharova O, Goryanin I, Artamonova D, Zyubko T, Shmakov S, Artamonova T, Khodorkovskii M, Severinov K. PpCas9 from Pasteurella pneumotropica – a compact Type II-C Cas9 ortholog active in human cells. Nucleic Acids Res. 2020 Dec 2;48(21):12297-12309. doi: 10.1093/nar/gkaa998
4. Fedorova I, Arseniev A, Selkova P, Pobegalov G, Goryanin I, Vasileva A, Musharova O, Abramova M, Kazalov M, Zyubko T, Artamonova T, Artamonova D, Shmakov S, Khodorkovskii M, Severinov K. DNA targeting by Clostridium cellulolyticum CRISPR-Cas9 Type II-C system. Nucleic Acids Res. 2020 Feb 28;48(4):2026-2034. doi: 10.1093/nar/gkz1225
Основные патенты:
1. RU2820345C1 «Средство обнаружения нуклеиновых кислот на основе ScCas12a белка из бактерии Sedimentisphaera cyanobacteriorum» (2024 год)
2. RU2804422C1 «Система редактирования геномной ДНК эукариотической клетки на основе нуклеотидной последовательности, кодирующей белок SuCas9NLS» (2023 год)
3. RU2778156C1 «Средство разрезания ДНК на основе Cas9 белка из бактерии Capnocytophaga ochracea» (2022 год)
4. RU2712497C1 «Средство разрезания ДНК на основе Cas9 белка из биотехнологически значимой бактерии Clostridium cellulolyticum» (2020 год)






- Разработка универсальной диагностической платформы на основе технологий CRISPR-Cas для выявления инфекционных заболеваний различной природы
Описание исследований
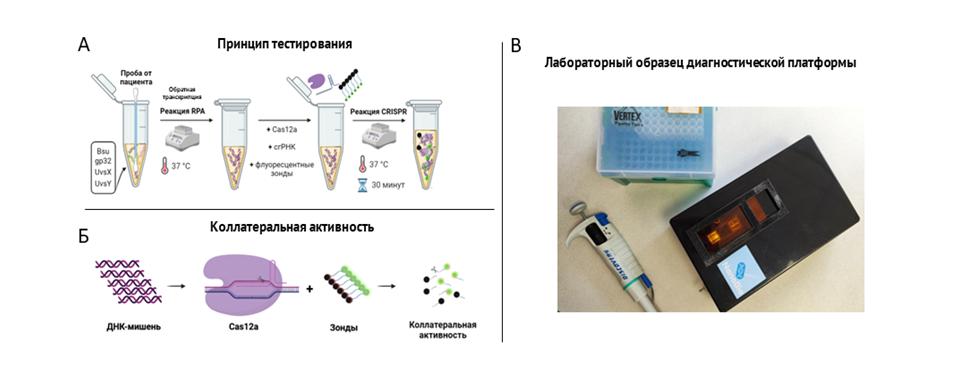
На сегодняшний день одним из основных вызовов человечеству является появление новых штаммов вирусов и бактерий. Для предотвращения распространения инфекций важно быстро и точно диагностировать их на ранних стадиях заболевания. Большинство используемых на сегодняшний день методов диагностики дороги, требуют наличия специализированного оборудования, а также сравнительно длительного времени для получения результатов диагностики.
Разрабатываемая в НИК "НаноБио" диагностическая платформа, основанная на реакции изотермической амплификации (RPA) и коллатеральной активности системы CRISPR-Cas, имеет чувствительность, сравнимую с ПЦР-РВ (103 копий), при этом относительно короткое время реакции (30-40 минут) и не требует дополнительного лабораторного оборудования, так как весь процесс тестирования проходит при фиксированной температуре (37-39°C). Это открывает широкие перспективы для её использования вне лаборатории без потери в точности диагностики.












- Исследование развития инфекции клеток гигантскими бактериофагами
Описание исследований
Бактериофаги - это вирусы бактерий, представляющие из себя вне бактериальной клетки молекулу нуклеиновой кислоты, упакованной в белковую оболочку. Когда же бактериофаг встречает бактерию, в которой может размножаться, то он переносит внутрь этой бактерии свою наследственную информацию, что запускает программу формирования новых фаговых частиц.Нашим основным объектом исследования является гигантский бактериофаг phiKZ и родственные ему фаги. За 60 минут, которые проходят с момента впрыска фаговой ДНК phiKZ до выхода новосинтезированных фаговых частиц, кардинально перестраиваютcя все процессы внутри клетки и существенно меняют морфологию бактерии: бактериальный нуклеоид меняет свое положение, уступая центральное место сферическому компартменту, напоминающий ядро эукариотической клетки. Данный компартмент покрыт белковой оболочкой, внутрь которой упаковывается фаговая ДНК и часть белков, участвующих в транскрипции и репликации, кроме того он удерживается в центре клетки за счет тубулин-подобных фаговых белков. Для транскрипции своего генома фаг phiKZ исключительно свои ДНК-зависимые РНК-полимеразы, которых у него две.
Наша группа изучает процессы, происходящие внутри клетки на фоне инфекции фагом phiKZ и механизмы, отвечающие за их осуществление.
Основные публикации:
1. Antonova D., Nichiporenko A., Sobinina M., Wang Y., Vishnyakov I., Moiseenko A., Kurdyumova I., Chesnokov Y., Stepanchikova E., Bourkaltseva M., Samygina V., Khodorkovskii M., Sokolova O., Yakunina M. Genomic transfer via membrane vesicle: a strategy of giant phage phiKZ for early infection // Journal of Virology. – 2024. – Vol. 98. №10 – P. e00205-24.
2. Nichiporenko A., Antonova D., Kurdyumova I., Khodorkovskii M., Yakunina M. Assembly of phiKZ bacteriophage Inner Body during infection // Biochemical and Biophysical Research Communications. – 2024. – Vol. 693 – P.149372.
3. Antonova D., Belousova V., Zhivkoplias E., Sobinina M., Artamonova T., Vishnyakov I., Kurdyumova I., Arseniev A., Morozova N., Severinov K., Khodorkovskii M., Yakunina M. The Dynamics of Synthesis and Localization of Jumbo Phage RNA Polymerases inside Infected Cells // Viruses. – 2023. – Vol.15. №10. – P. 2096.
4. Natàlia de Martín Garrido, Orekhova M., Yuen Ting Emilie Lai Wan Loong, Anna Litvinova, Kailash Ramlaul, Tatyana Artamonova, Alexei S Melnikov, Pavel Serdobintsev, Christopher H S Aylett, Maria Yakunina. Structure of the bacteriophage PhiKZ non-virion RNA polymerase, Nucleic Acids Research, 2021, Volume 49, Volume 49, Issue 13, P. 7732–7739, doi: 10.1093/nar/gkab539
5. Danilova Y.A.; Belousova V.V.; Moiseenko A.V.; Vishnyakov I.E.; Yakunina M.V.; Sokolova O.S. Maturation of Pseudo-Nucleus Compartment in P. aeruginosa, Infected with Giant phiKZ Phage, Viruses 2020, 12, 1197
6. Orekhova, M., Koreshova, A., Artamonova, T., Khodorkovskii, M., Yakunina, M. The study of the phiKZ phage non-canonical non-virion RNA polymerase, Biochemical and Biophysical Research Communications, 2019, doi: 10.1016/j.bbrc.2019.02.132
7. Lavysh D, Sokolova M, Minakhin L, Yakunina M, Artamonova T, Kozyavkin S, Makarova KS, Koonin EV, Severinov K. The genome of AR9, a giant transducing Bacillus phage encoding two multisubunit RNA polymerases, Journal of Virology – 2016. – Vol. 495. – P. 185-196.
8. Yakunina M, Artamonova T, Borukhov S, Kira S. Makarova, Severinov K, Minakhin, L. A non-canonical multisubunit RNA polymerase encoded by a giant bacteriophage, Nucleic Acids Research. - 2015. - Vol. 43. – P. 10411-10420.





- Одномолекулярные исследования ДНК-белковых взаимодействий
Описание исследований
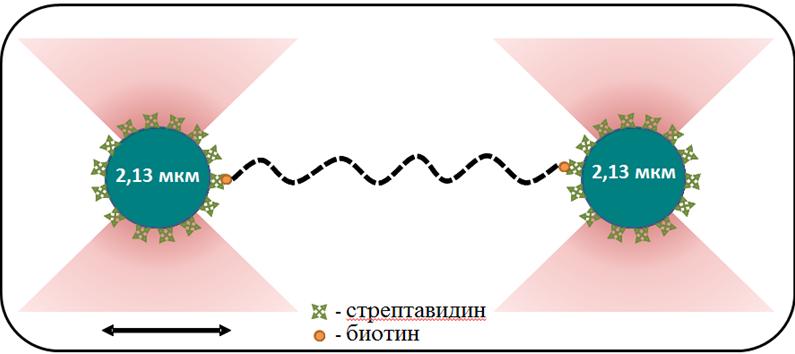
Группа фокусируется на исследованиях ДНК-белковых взаимодействий при помощи метода оптического захвата, реализованного на установке Лазерный пинцет. Комбинация метода оптического захвата с микрофлюидной системой ламинарных потоков позволяет отслеживать изменения механических свойств индивидуальных молекул ДНК в ходе взаимодействия с ДНК-связывающими белками. При помощи метода оптического захвата наша группа изучает свойства нуклеопротеиновых комплексов, формируемых бактериальным белком RecA (E. coli, D. radiodurans) на дуплексной и однонитевой (одноцепочечной) молекулах ДНК. В бактериях RecA в виде нуклеопротеинового филамента, формируемого на однонитевой ДНК, участвует сразу в нескольких ключевых процессах: репарации тяжелых повреждений ДНК, передаче генов устойчивости к антибиотикам, запуске SOS-ответа. Считается известным, что в зависимости от типа связанного нуклеотидного кофактора филамент RecA на однонитевой ДНК может находиться в активной или неактивной конформации. Для поддержания активной конформации филамента необходимо наличие в среде свободной АТФ. АТФазная активность RecA потенциально приводит к локальному возникновению участков неактивной конформации в структуре филамента, в целом обладающего активной конформацией. Нашей группой проводятся исследования конформационных перестроек и состояний филамента RecA а также регуляции активности RecA белковыми кофакторами.
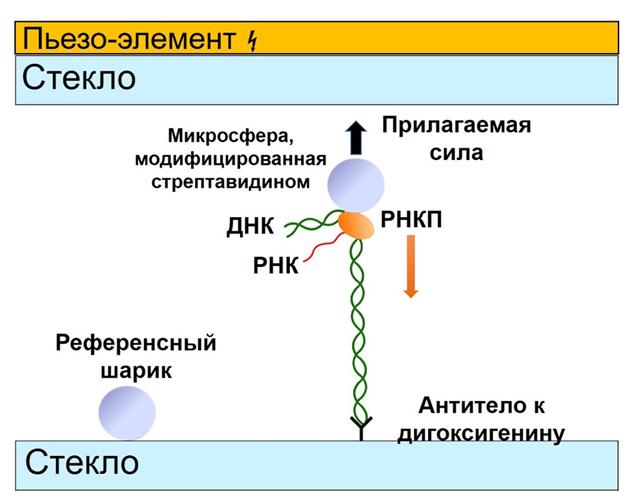
Группа также занимается исследованиями бактериальной транскрипции и её регуляции на уровне одиночных молекул в режиме реального времени, применяя метод акустической силовой спектроскопии. Мы являемся первыми в мире, кто успешно применил этот одномолекулярный подход для изучения процессов транскрипции. Разработанная методика позволила выявить характер ингибирования новых лассо-пептидов ацинетодина и клебсидина. На данный момент мы подготавливаем публикацию, в которой представлен уникальный способ синергетического ингибирования РНК-полимеразы антибиотиком стрептолидигином совместно с транскрипционными факторами GreA и GreB. Наши исследования в этой области не только расширяют понимание молекулярных механизмов бактериальной транскрипции, но также могут иметь важные практические применения в разработке новых антимикробных препаратов
Основные публикации:
1. Alekseev A., Pobegalov G., Morozova N., Vedyaykin A., Cherevatenko G., Yakimov A., Baitin D., Khodorkovskii M., A new insight into RecA filament regulation by RecX from the analysis of conformation-specific interactions, eLife, 2022, V. 11, e78409
2. Alekseev, A., Serdakov, M., Pobegalov, G., Yakimov, A., Bakhlanova, I., Baitin, D., Khodorkovskii, M. Single‐molecule analysis reveals two distinct states of the compressed RecA filament on single‐stranded DNA. FEBS letters, 2020, 594(21), 3464-3476.
3. Alekseev, A., Cherevatenko, G., Serdakov, M., Pobegalov, G., Yakimov, A., Bakhlanova, I., Baitin, D., Khodorkovskii, M. Single-Molecule Insights into ATP-Dependent Conformational Dynamics of Nucleoprotein Filaments of Deinococcus radiodurans RecA. International journal of molecular sciences, 2020, 21(19), 7389.
4. Alekseev A., Morozova N., Vedyaykin A., Yakimov A., Khodorkovskii M., Pobegalov G., Single-molecule characterization of compressed RecA nucleoprotein filaments, Biochemical and Biophysical Research Communications, 2022, V. 614, pp. 29-33
5. Yakimov, A., Pobegalov, G., Bakhlanova, I., Khodorkovskii, M., Petukhov, M., Baitin, D. Blocking the RecA activity and SOS-response in bacteria with a short α-helical peptide. Nucleic acids research, 2017, 45(16), 9788-9796.
6. Pobegalov, G, Cherevatenko, G., Alekseev, A., Sabantsev, A., Kovaleva, O., Vedyaykin, A., Morozova, N., Baitin, D., Khodorkovskii, M. Deinococcus radiodurans RecA nucleoprotein filaments characterized at the single-molecule level with optical tweezers. Biochemical and biophysical research communications, 2015, 466(3), 426-430.
7. Metelev M, Arseniev A, Bushin LB, Kuznedelov K, Artamonova TO, Kondratenko R, Khodorkovskii M, Seyedsayamdost MR, Severinov K. Acinetodin and Klebsidin, RNA Polymerase Targeting Lasso Peptides Produced by Human Isolates of Acinetobacter gyllenbergii and Klebsiella pneumoniae. ACS Chem Biol. 2017 Mar 17;12(3):814-824




- Изучение молекулярных механизмов систем рестрикции-модификации и других защитных систем бактерий от вирусов на уровне одиночных бактериальных клеток
Описание исследований
В живой природе бактерии постоянно подвергаются заражению вирусами, которых называют бактериофагами. Такие вирусы способны чрезвычайно эффективно уничтожать целые бактериальные популяции. Для своей защиты от вирусной инфекции бактерии выработали множество молекулярных механизмов, действующих на совершенно разные части бактериофага на разных стадиях его развития в клетке.
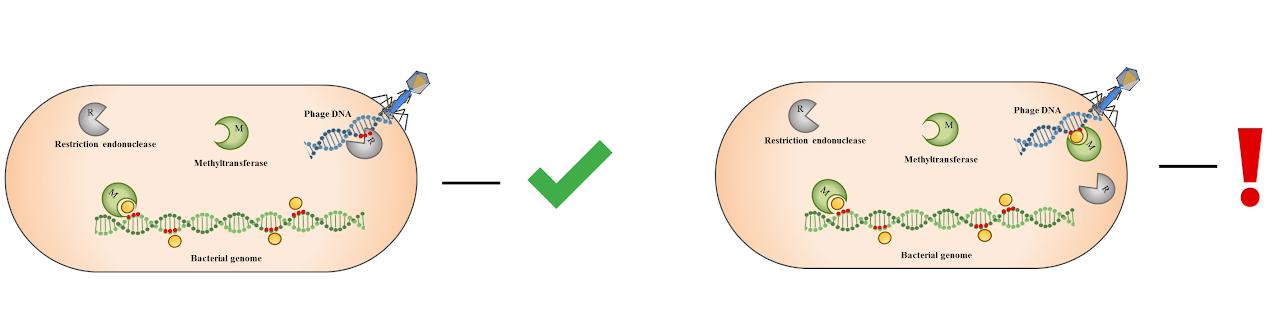
Одними из самых распространённых защитных систем бактерий являются системы рестрикции-модификации. Такие системы действуют за счёт активности эндонуклеазы рестрикции, которая вносит двунитевой разрыв в специфические сайты узнавания на ДНК и метилтрансферазной активности, которая метилирует геном бактерии, защищая его от деградации эндонуклеазой рестрикции. Несмотря на высокий уровень защиты, обеспечиваемый этими системами, в некоторых случаях ДНК инфицирующего бактериофага избегает деградации и подвергается модификации. В результате возникает модифицированное вирусное потомство, полностью устойчивое к действию системы рестрикции-модификации.
Мы изучаем влияние вариации экспрессии генов систем рестрикции-модификации на эффективность защиты одиночных бактерий от вируса. Также мы занимаемся изучением механизмов работы других систем защиты бактерий от вируса на уровне одиночных бактерий.
Основные публикации:
1. Morozova N, Sabantsev A, Bogdanova E, Fedorova Y, Maikova A, Vedyaykin A, et al. Temporal dynamics of methyltransferase and restriction endonuclease accumulation in individual cells after introducing a restriction-modification system. Nucleic Acids Research, 2016, 44(2), 790-800. DOI: 10.1093/nar/gkv1490.
2. A. Strotskaya, E. Savitskaya, A. Metlitskaya, N. Morozova, K. Datsenko, E. Semenova, K. Severinov. The action of Escherichia coli CRISPR–Cas system on lytic bacteriophages with different lifestyles and development strategies. Nucleic Acids Research, 2017, 45(4), 1946-1957. DOI: 10.1093/nar/gkx042.
3. B. Wilcox, I. Osterman, M. Serebryakova, D. Lukyanov, E. Komarova, B. Gollan, N. Morozova, Yu. Wolf, K. Makarova, S. Helaine, P. Sergiev, S. Dubiley, S. Borukhov, K. Severinov. Escherichia coli ItaT is a type II toxin that inhibits translation by acetylating isoleucyl-tRNAIle. Nucleic Acids Research, 2018, 46(15), 7873–7885. DOI: 10.1093/nar/gky560.
4. Smirnov, S.V., Morozova, N.E., Khodorkovskii, M.A., Severinov, K.V. Fluorescence microscopy study of the effect of Esp1396I restriction-modification system proteins concentrations on protection against lambda phage. Journal of Physics: Conference Series, 2018, 1135(1), 012016. DOI: 10.1088/1742-6596/1135/1/012016.
5. J. Gordeeva, N. Morozova, N. Sierro, A. Isaev, T. Sinkunas, K. Tsvetkova, M. Matlashov, L. Truncaitė, R.D. Morgan, N.V. Ivanov, V. Siksnys, L. Zeng, K. Severinov. BREX system of Escherichia coli distinguishes self from non-self by methylation of a specific DNA site. Nucleic Acids Research, 2019, 47(1), 253–265. DOI: doi.org/10.1093/nar/gky1125.
6. Antonova, D.A., Morozova, N.E., Shiryaeva, A.A., Khodorkovskii, M.A. Regulation of type II restriction-modification system Esp1396I. Journal of Physics: Conference Series, 2019, 1400(3), 033024. DOI: 10.1088/1742-6596/1400/3/033024.
7. Znobishcheva, E.A., Morozova, N.E., Khodorkovskii, M.A. Fluorescent labeling of bacteriophage T7 by CRISPR-Cas9. Journal of Physics: Conference Series, 2019; 1400(3), 033005. DOI: 10.1088/1742-6596/1400/3/033005.




- Изучение комплексов SMC и белков деления бактерий
Описание исследований
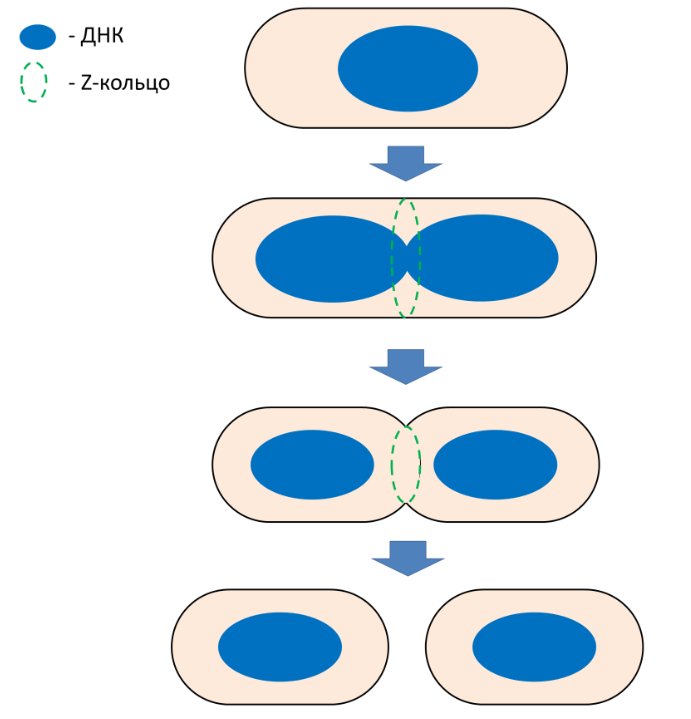
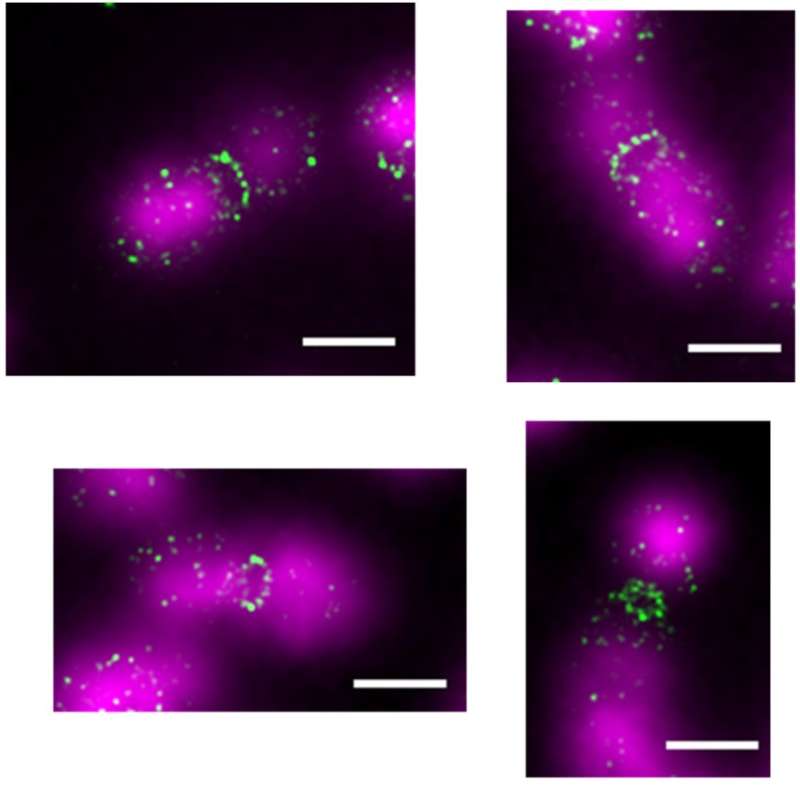
Цитоскелет – это белковый «каркас» клетки. Долгое время белки цитоскелета считались принадлежностью лишь эукариотических клеток – действительно, зачем бактериям цитоскелет, если они покрыты жесткой клеточной стенкой? Тем не менее, за последние 30 лет у бактерий были обнаружены гомологи всех основных белков цитоскелета эукариот – актина, тубулина и промежуточных филаментов. Эти белки в бактериях принимают участие в различных жизненно важных процессах, в том числе в поддержании формы клетки, сегрегации молекул ДНК, клеточном делении. Одним из важнейших белков бактериального цитоскелета является FtsZ – ключевой белок деления, являющийся гомологом тубулина. Как именно белок FtsZ участвует в делении бактерий? Многое об этом ещё неизвестно, однако в хорошо изученных видах бактерий, например, в Escherichia coli, роль белка FtsZ в целом ясна. FtsZ в клетке полимеризуется и формирует Z-кольцо, которое является каркасом, своеобразными «строительными лесами» для других белков деления. Именно эти белки, как считается, выполняют основную работу по строительству перегородки между будущими дочерними клетками и некоторые другие функции, а FtsZ лишь направляет эти белки, обеспечивая их слаженную работу. Однако не следует полагать, что о делении бактерий уже всё известно. Какова точная структура Z-кольца? Деформируют ли полимеры FtsZ оболочку клетки? Как делятся бактерии, у которых нет белка FtsZ? На эти и многие другие вопросы ещё предстоит найти ответы. Наша группа занимается изучением свойств белка FtsZ: мы визуализируем структуры, которые формирует этот белок в бактериальных клетках и в пробирке; определяем, с какими белками он взаимодействует; выясняем, чем отличаются роли и функции белка FtsZ в разных видах бактерий. Кроме того, мы имеем цель выяснить, как делятся бактерии, которые не имеют белка FtsZ. Наконец, нам интересны белки бактерий, которые формируют цитоскелет-подобные структуры.
Белковые комплексы типа SMC (от англ. Structural maintenance of chromosomes, далее в тексте - комплексы SMC) являются ключевыми участниками пространственной организации ДНК во всех живых организмах - в бактериях, археях и эукариотах. В бактериях имеется несколько гомологов комплексов SMC, которые выполняют, на первый взгляд, несвязанные друг с другом функции, однако действуют, по-видимому, посредством очень похожих между собой, консервативных механизмов. За последние годы установлено, что комплексы SMC способны осуществлять формирование петель из ДНК (так называемую экструзию петель), что позволяет рассматривать их как отдельный класс ДНК-транслоказ. Интересно отметить, что ключевое свойство для комплексов SMC – экструзия петель – до сих пор напрямую не продемонстрировано для комплексов SMC бактерий, в отличие от комплексов SMC эукариот. Точный механизм экструзии пока не установлен, но было предложено несколько моделей, которые требуют экспериментального подтверждения. Для комплексов SMC, в том числе бактериальных, имеется множество вопросов, среди которых, кроме механизма экструзии петель, одним из наиболее важных вопросов является полный состав комплексов SMC, включая регуляторные белки, активирующие или ингибирующие активность комплексов. До сих пор неясно, какие именно факторы управляют работой SMC-подобных комплексов - например, обеспечивают согласование их работы с клеточным циклом, а также позволяют осуществлять параллельную работу нескольких видов комплексов SMC в одной клетке. Бактерии устроены более просто, имеют меньшее число видов комплексов SMC и, вероятно, меньшее число факторов, регулирующих работу этих комплексов, поэтому изучение бактериальных SMC-подобных комплексов представляется более простой задачей, которая может дать ответы на вопросы, справедливые для комплексов SMC в целом. Наша группа проводит комплексное исследование нескольких видов бактериальных комплексов типа SMC.
Основные публикации:
1. Rumyantseva N.A., Sapozhnikova A.P., Khasanova A.A., Zapryagaeva E.Yu., Kudryavtseva M.A., Morozova N.E., Vedyaykin A.D. Ureaplasma parvum SMC-ScpAB complex is capable of loop extrusion and demonstrates properties that distinguish it from Bacillus subtilis homologue. // Archives of Biochemistry and Biophysics, 2025. 774: 110641. DOI: 10.1016/j.abb.2025.110641
2. Roshektaeva V.D., Alekseev A.A., Vedyaykin A.D., Vinnik V.A., Baitin D.M., Bakhlanova I.V., Pobegalov G.E., Khodorkovskii M.A., Morozova N.E. Features of the DNA Escherichia coli RecN interaction revealed by fluorescence microscopy and single-molecule methods. // Biochemical and Biophysical Research Communications, 2024. 716: p. 150009. DOI: 10.1016/j.bbrc.2024.150009
3. Rumyantseva N.A., Golofeeva D.M., Vedyaykin A.D. SulA does not sequester FtsZ in Escherichia coli cells during the SOS response. // Biochemical and Biophysical Research Communications, 2024. 691: p. 149313. https://www.sciencedirect.com/science/article/pii/S0006291X23014079?via%3Dihub DOI: 10.1016/j.bbrc.2023.149313
4. Rumyantseva N.A., Golofeeva D.M., Shabalina A.V., Vedyaykin A.D. Direct evidence of the ability of Pseudomonas aeruginosa and E. coli SulA to dimerize. // Archives of Biochemistry and Biophysics, 2024. 751: p. 109826. https://www.sciencedirect.com/science/article/pii/S0003986123003259 DOI: 10.1016/j.abb.2023.109826
5. Н. А. Румянцева, Д. М. Голофеева, А. А. Хасанова, А. Д. Ведяйкин. Гомологи тубулина бактерий и архей. // Микробиология, 2024. 93. № 3. 249-266. https://link.springer.com/article/10.1134/S002626172460469X DOI: 10.1134/S002626172460469X.
6. Морозова Н.Е., Потысьева А.С., Ведяйкин А.Д. Особенности структуры и функций бактериальных комплексов SMC. Цитология. 2023. Т. 65, № 6 С. 522-534. https://journals.rcsi.science/0041-3771/article/view/232793 DOI: S004137712306007X.








- Исследование белка RecN - SMC-подобного компонента бактериального SOS- ответа
Описание исследований
RecN является одним из факторов SOS-ответа - процесса, возникающего в бактериальной клетке в ответ на повреждение ДНК. Причиной таких повреждений, в частности, может быть облучение излучением УФ-диапазона или воздействие различного рода антибактериальных агентов. Результатом активации SOS-ответа может являться точное восстановление поврежденных участков ДНК, а также адаптация бактерии к повреждающему воздействию, за счет повышенного мутагенеза в клетках бактерий. Важно отметить, что за счет этого SOS-ответ представляет собой основной механизм адаптации бактерий к действию антибиотиков.
Белок RecN экспрессируется и действует на ранней стадии SOS-ответа, и согласно данным, полученным in vivo, является одним из ключевых факторов успешного протекания данного процесса. Установлено, что RecN относится к SMC-белкам (Structural Maintenance of Chromosomes) - семейству АТФаз, принимающих участие в динамическом регулировании организации структуры хромосом. SMC-белки обладают высокой консервативностью как среди прокариот, так и эукариот.



- Кинетика сверхбыстрых процессов в молекулах и кластерах
Описание исследований
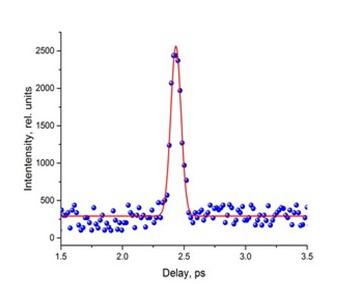
Для исследования быстро протекающих процессов используются импульсы света фемтосекундной длительности. Такие импульсы создаются с помощью фемтосекундного лазера на титан-сапфире. Лазерные импульсы (800нм) преобразуются с помощью генератора гармоник (400 и 266 нм) и генератора белого света (излучение суперконтинуума 400-1000 нм). Измерения проводятся методом «возбуждение-зондирование» с помощью линии оптической задержки. Первый импульс приводит к возбуждению объекта, второй импульс приходит к объекту с задержкой и используется для анализа состояния в котором находится объект. Изменяя задержку можно получить информацию о процессах происходящих в исследуемом объекте.
В нашей группе проводятся исследования быстропротекающих процессов в люминесцентных зондах и кластерах инертных газов. Отметим, что при использовании лазерных фемтосекундных импульсов легко наблюдаются различные нелинейные оптические процессы, в частности многофотонное поглощение.
Люминесцентные зонды широко используются для измерения различных параметров (температура, концентрация кислорода, pH) в биологических исследованиях, медицине, аэрокосмической промышленности и микроэлектронике. Люминесцентный зонд это молекула (или частица) оптические свойства которой сильно зависят от измеряемой величины. Как правило измеряется интенсивность свечения или время жизни возбуждённого состояния.
Одним из способов значительного улучшения свойств люминесцентных зондов является использование их в составе молекулярных диад. Молекулярная диада представляет собой два хромофорных центра, соединённых небольшим ковалентным мостиком. В такого типа молекулярных системах после возбуждения одного хромофорного центра возможен перенос энергии между хромофорами. Использование молекулярных диад, где хромофоры имеют разные функции и обмениваются энергией позволяет варьировать свойства систем в целом (изменить положение полос поглощения и/или эмиссии, увеличить/уменьшить диапазон измерений и.т.д.). Наши исследования направлены на определение механизмов передачи энергии в молекулярных диадах, находящихся в электронно-возбуждённом состоянии.
Кластеры инертных газов являются удобным объектом модельным объектом для изучения процессов релаксации в многоатомных системах. Для целого ряда многоатомных систем, находящихся в электронно-возбуждённом состоянии основным механизмом релаксации являются безызлучательные процессы. Как правило, их скорость значительно превышает скорость радиационного распада. В многоатомных молекулах со сравнительно большими энергиями связи между атомами основным и часто единственным механизмом безызлучательной релаксации является электронно-колебательное взаимодействие. В кластерах (многоатомных молекулах, нанокаплях) со сравнительно небольшими энергиями связи между атомами появляются дополнительные каналы релаксации (десорбция атомов, ионизация, фрагментация). При этом доминирующий канал релаксации зависит не только от энергии связи между атомами, но и от размера объекта и энергии возбуждения. Несмотря на активное изучение данных процессов в кластерах даже качественные механизмы релаксации на сегодняшний день не всегда ясны. В кластерах ксенона нами был обнаружен ICD-подобный процесс. Данный процесс возможен при одновременном возбуждении двух атомов входящих в кластер. Перенос энергии между двумя соседними возбужденными атомами приводит к ионизации кластера. Характерное время ионизации кластера ксенона в этом процессе составляет ~ 5 пс.



Основные публикации:
1. P.Y. Serdobintsev, A.S. Melnikov, A.A. Pastor, N.A. Timofeev, M.A. Khodorkovskiy, J. Chem. Phys., 2018, V.148, 194301
2. I. Balmaev, P. Serdobintsev, A. Melnikov, A. Pastor, M. Khodorkovskiy, Journal of Physics: Conference Series 1410 (1), 012135
3. Kisel K.S., Melnikov A.S., Grachova E.V., Hirva P., Tunik S. P., Koshevoy I.O., Chemistry–A European Journal, 2017, V.23, P.11301-11311
4. Belyaev A., Kolesnikov I., Melnikov A.S., Gurzhiy V.V., Tunik S.P., Koshevoy I.O., New Journal of Chemistry, 2019, V.43, P.13741-13750



